Glejak wielopostaciowy to jeden z najtrudniejszych przeciwników współczesnej onkologii – wymyka się tradycyjnym metodom leczenia i nowoczesnej immunoterapii. W projekcie SelCell naukowcy Łukasiewicz – PORT szukają rozwiązania w limfocytach T gamma-delta i sprawdzają, co sprawia, że komórki odpornościowe jednego dawcy niszczą nowotwór skuteczniej niż inne.
Wyzwanie – przełamać opór mikrośrodowiska
Glejak wielopostaciowy to nowotwór mózgu, który poprzez swoją lokalizację tworzy barierę dla standardowych leków. Dodatkowo jego środowisko działa silnie immunosupresyjnie, „wyłączając” układ odpornościowy pacjenta. Statystyki są nieubłagane – 5-letnie przeżycie wynosi zaledwie 5,1%.
Nadzieją współczesnej onkologii stała się immunoterapia, w tym przełomowe komórki CAR-T. Dzięki inżynierii genetycznej limfocyty T pacjenta przekształcane są w inteligentny „żywy lek” zdolny do precyzyjnego namierzenia i niszczenia nowotworu. Choć metoda ta odnosi sukcesy w leczeniu nowotworów krwi, takich jak białaczka czy chłoniaki, w przypadku guzów litych – a do nich właśnie zalicza się glejak – jej skuteczność jest ograniczona. Barierą pozostaje też wymóg izolacji i modyfikacji limfocytów T od pacjenta, czasochłonny proces produkcji i wysoki koszt.
Dlatego w projekcie SelCell realizowanym w Łukasiewicz – PORT naukowcy stawiają na limfocyty T gamma-delta (γδ) i to w nich widzą szansę na nową formę leczenia nowotworów litych.
Dlaczego limfocyty T γδ?
Stanowią zaledwie 1-10% wszystkich limfocytów krążących w ludzkiej krwi, ale mają kluczowe przewagi nad komórkami stosowanymi w terapii CAR-T.
– Nie wymagają zgodności tkankowej, czyli nie muszą pochodzić od pacjenta. Można je pobrać od zdrowego dawcy i podać niespokrewnionemu z nim pacjentowi bez ryzyka, że zaatakują jego zdrowe narządy – wyjaśnia dr hab. Grzegorz Chodaczek kierujący projektem i Grupą Badawczą Immunoterapii w Łukasiewicz – PORT. – „Nasze” limfocyty są z natury cytotoksyczne. Rozpoznają tzw. antygeny stresu, czyli konkretne białka obecne tylko na powierzchni komórek nowotworowych. Łącząc się z nimi, doprowadzają do ich śmierci – to właśnie w tym mechanizmie leży potencjał terapeutyczny limfocytów T gamma-delta.

W poszukiwaniu idealnego dawcy
Wcześniejsze badania zespołu wykazały, że aktywność cytotoksyczna limfocytów zależy od konkretnego dawcy. W projekcie finansowanym przez Agencję Badań Medycznych naukowcy Łukasiewicz – PORT chcą zrozumieć, dlaczego komórki od jednych osób są „super-zabójcami” nowotworów, a od innych działają znacznie słabiej.
Dzięki współpracy z Regionalnym Centrum Krwiodawstwa i Krwiolecznictwa we Wrocławiu zespół ma dostęp do materiału biologicznego od zdrowych osób, z którego izoluje i namnaża dwie populacje limfocytów T gamma-delta, a następnie testuje je na panelu siedmiu linii komórkowych glejaka.
– Szukamy molekularnego „podpisu” dawcy i hodowli limfocytów o najlepszych właściwościach przeciwnowotworowych. Nikt do tej pory nie wyjaśnił, który podtyp komórek T gamma-delta jest bardziej skuteczny i jaki rodzaj receptora decyduje o ich zdolnościach do zabijania glejaka – tłumaczy dr hab. Grzegorz Chodaczek, którego grupa w poszukiwaniu odpowiedzi na te pytania wykorzystuje wysoce specjalistyczną aparaturę.
Technologia, która widzi więcej
Unikalny proces technologiczny, tzw. „pipeline”, pozwala na precyzyjną i wielowymiarową charakterystykę procesu walki z rakiem. Podstawą badań jest masowa hodowla komórkowa w dedykowanym inkubatorze, który zapewnia identyczne i stabilne środowisko dla komórek pochodzących od wielu dawców. To kluczowe dla wiarygodności wyników.
Kolejnym etapem jest głębokie fenotypowanie wykorzystujące zaawansowaną cytometrię spektralną. Technologia ta, w przeciwieństwie do klasycznych metod, pozwala naukowcom analizować nawet 40 markerów jednocześnie, dając niezwykle szczegółowy obraz kondycji komórek, obecności rzadkich receptorów aktywacyjnych czy ich stanu wyczerpania.
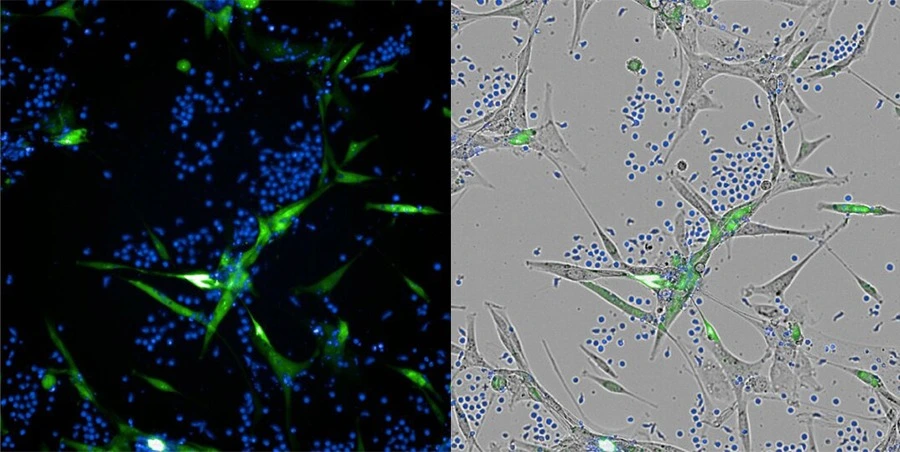
Integralną częścią procesu jest system do mikroskopii wysokoprzepustowej, który umożliwia wizualizację zabijania komórek nowotworowych w czasie rzeczywistym. Badacze mogą dzięki niemu śledzić dynamikę procesu, rejestrować chwilę śmierci komórek glejaka pod wpływem limfocytów, a przede wszystkim uzyskać dane liczbowe umożliwiające porównanie aktywności hodowli od różnych dawców.
Całość dopełniają analizy transkryptomiczne i proteomiczne z wykorzystaniem sekwencjonowania nowej generacji i spektrometrii mas. Tu badane są aktywowane geny i białka produkowane przez najskuteczniejsze limfocyty. Pozwala to lepiej zrozumieć molekularne podłoże ich efektywności i wyznaczać nowe cele terapeutyczne.
– W immunoterapii guzów litych nauka stoi przed murem, którego klasyczne metody nie potrafią jeszcze przebić. Dzięki tak rozbudowanej platformie technologicznej nie szukamy nowego rozwiązania na ślepo. Nie tylko widzimy, które komórki zabijają nowotwór, ale zaczynamy też rozumieć, dlaczego to robią – dodaje dr hab. Grzegorz Chodaczek.
Od probówki do awatara pacjenta
Celem projektu jest stworzenie uniwersalnego standardu selekcji dawców posiadających najbardziej skuteczne limfocyty, co otworzy drogę do przekształcenia biologicznego potencjału limfocytów γδ w skuteczną formę terapii. Zanim to jednak nastąpi, przed Grupa Badawczą Immunoterapii stoją kolejne wyzwania do realizacji w innych projektach.
W następnym kroku konieczna jest weryfikacja wyników w bardziej zaawansowanych modelach in vivo. Naukowcy planują odtworzyć ludzki układ odpornościowy w modelowych organizmach, aby badać interakcje limfocytów z guzem w środowisku maksymalnie zbliżonym do organizmu pacjenta, uwzględniającym specyficzne, immunosupresyjne mikrośrodowisko nowotworu.
Realizacja projektu SelCell stanowi zatem kluczowy, niezbędny etap na ścieżce rozwoju innowacyjnego produktu leczniczego opartego na limfocytach T gamma-delta, prowadzący od badań podstawowych do przyszłych zastosowań klinicznych.




