Przez ponad sto lat nauka wierzyła, że za nasze myśli, emocje i pamięć odpowiadają neurony. Resztę mózgu traktowano jak mało istotne wypełnienie. Z okazji Tygodnia Wiedzy o Mózgu opowiadamy o wciąż mało znanych bohaterach drugiego planu – astrocytach. Badania pokazują, że te komórki w kształcie gwiazd mogą być kluczem do zrozumienia takich chorób jak depresja czy choroba Alzheimera.
100 lat w cieniu neuronów
W 1856 roku niemiecki lekarz Rudolf Virchow opisał i nazwał substancję znajdującą się pomiędzy neuronami „Nervenkitt”, czyli klej nerwowy – nieistotne wypełnienie. Czterdzieści lat później węgierski anatom Michael von Lenhossek przyjrzał się tym komórkom pod mikroskopem i dostrzegł ich gwiaździsty kształt. Nazwał je astrocytami – od greckiego słowa „astron”, oznaczającego gwiazdę.
Przez ponad sto lat wiedza naukowa o astrocytach zmieniała się niewiele: wiadomo było, że utrzymują odpowiednie środowisko chemiczne dla neuronów, regulują stężenie jonów i usuwają odpady metaboliczne. Ważne i potrzebne, ale nie aż tak istotne, by stanowiły główny przedmiot badań.
Dopiero w ostatniej dekadzie XX wieku badacze odkryli, że astrocyty komunikują się z neuronami i nie są biernymi obserwatorami, lecz aktywnymi uczestnikami procesów zachodzących w mózgu. Komórki te „podsłuchują” rozmowy neuronów i mogą je modulować. Od tego momentu astrocyty zaczęły przyciągać coraz większą uwagę naukowców, jednak prawdziwa rewolucja w ich badaniach nastąpiła dopiero w ostatnich latach.
Przełomowe lata w badaniach nad astrocytami
Lata 2025 i 2026 przyniosły bezprecedensową serię odkryć opublikowanych w najważniejszych czasopismach naukowych świata. Oto kilka z nich, które zmieniają obraz neurobiologii i kierunek dalszych badań.
Astrocyty – druga kopia zapasowa wspomnień
Do niedawna uważano, że pamięć jest wyłączną domeną neuronów. Badania zespołów prof. Inbal Goshen oraz Benjamina Deneena pokazały jednak, że astrocyty mogą tworzyć własne ślady pamięciowe. Podczas uczenia się niewielka grupa tych komórek – około 2–4% – aktywuje się równolegle z neuronami, potencjalnie tworząc dodatkową kopię naszych wspomnień.
Badanie opublikowane w lutym 2026 roku w czasopiśmie „Nature” wykazało ponadto kluczową rolę astrocytów w ciele migdałowatym w powstawaniu i utrzymywaniu pamięci strachu – zjawiska bezpośrednio związanego z obszarem badań prowadzonych w programie P4Health. Autor tych odkryć, dr Andrew Holmes, prezentował swoje wyniki podczas konferencji PORT for Health: Neuroscience 2023.
Norepinefryna – koncentracja potrzebuje pośrednika
Przez dekady sądzono, że norepinefryna – neuroprzekaźnik odpowiedzialny za czujność i koncentrację – działa bezpośrednio na neurony. Niedawna seria badań opublikowanych w „Science” obaliła ten dogmat: norepinefryna oddziałuje najpierw na astrocyty, a dopiero potem astrocyty wpływają na neurony.
Ryby, którym laserowo „wyłączono” astrocyty, traciły zdolność zatrzymywania się, ponieważ norepinefryna nie mogła już bezpośrednio przekazać takiego sygnału neuronom. Badania dr. Michała Ślęzaka z Łukasiewicz – PORT wykazały ponadto, że sygnalizacja noradrenaliny w astrocytach jest niezbędna, aby komórki te mogły odbierać sygnały z synaps.
Białko CCN1 – kontrola plastyczności mózgu
Artykuł opublikowany w „Nature” ujawnił, że białko CCN1, produkowane przez astrocyty, odpowiada za stabilność połączeń w dorosłym mózgu. Bez niego neurony tracą swoje stałe punkty oparcia i zaczynają tworzyć przypadkowe, krótkotrwałe połączenia, co prowadzi do degradacji takich obszarów jak ośrodek wzroku.
Gdyby nauka i medycyna nauczyły się kontrolować poziom CCN1, możliwe byłoby przywrócenie dorosłemu mózgowi dziecięcej plastyczności. Otworzyłoby to zupełnie nowe możliwości w rehabilitacji po urazach neurologicznych czy udarach.
Architektura astrocytów – nawet milion połączeń
Publikacja w czasopiśmie „Cell” pokazała niezwykłą architekturę astrocytów. Każdy z nich posiada tysiące mikroskopijnych wypustek (tzw. liści), które są około 400 razy cieńsze od ludzkiego włosa. Pojedynczy astrocyt może jednocześnie otaczać nawet milion synaps.
Działa wówczas jak biologiczny procesor – zbiera rozproszone sygnały z tysięcy neuronów i porządkuje je w spójną informację.
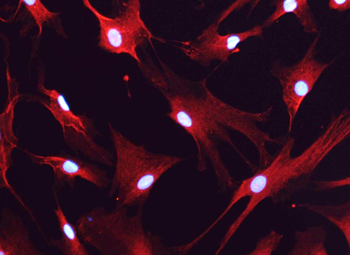
Rola astrocytów w depresji
Zmiana paradygmatu w myśleniu o mózgu jest szczególnie widoczna w badaniach nad chorobami psychicznymi. Zespół dr. Michała Ślęzaka wykazał, że zaburzenia funkcjonowania astrocytów – a nie tylko neuronów – mogą odgrywać kluczową rolę w rozwoju depresji.
Komórki te są głównym odbiorcą hormonów stresu, czyli glikokortykoidów, w naszym układzie nerwowym i jako pierwsze reagują na niekorzystne doświadczenia organizmu. Gdy stres staje się przewlekły, procesy metaboliczne w astrocytach ulegają zaburzeniu, co prowadzi do nieprawidłowej pracy neuronów w obszarach mózgu odpowiedzialnych za regulację emocji.
Badania prowadzone we współpracy z przemysłem farmaceutycznym wykazały, że specyficzny profil genetyczny astrocytów był najważniejszą cechą odróżniającą próbki mózgów osób, które zmarły w wyniku samobójstwa, od próbek zdrowych osób. Problem jest poważny, ponieważ w astrocytach zbiegają się kluczowe szlaki energetyczne oraz procesy produkcji najważniejszych neuroprzekaźników. Glutaminian i GABA pełnią rolę głównego „akceleratora” i „hamulca” sygnalizacji nerwowej, dlatego równowaga między nimi leży u podstaw praktycznie każdej funkcji mózgu – od stabilności nastroju po zdolność koncentracji.
– Przewlekły stres zaburza ten delikatny mechanizm. Wprowadza chaos w komunikacji między neuronami i komórkami glejowymi, a przerwanie tego dialogu prowadzi do zmian w programie molekularnym obu typów komórek. Dlatego zrozumienie zaburzeń funkcji astrocytów jest kluczowe dla opracowania skuteczniejszych terapii depresji – mówi dr Ślęzak, lider Grupy Badawczej Biologii Astrocytów.
Przywrócenie równowagi w chorym mózgu mogłoby otworzyć drogę do nowych terapii dla milionów pacjentów, u których obecnie dostępne leki nie przynoszą poprawy.
Astrocyty a choroby neurodegeneracyjne
Jedną z kluczowych funkcji komórek jest utrzymywanie tzw. kontroli jakości białek – systemu wykrywającego i usuwającego nieprawidłowo zbudowane cząsteczki. W zdrowym mózgu wadliwe białka są stale naprawiane lub usuwane. Gdy zaczynają się gromadzić, tworzą toksyczne osady charakterystyczne dla chorób neurodegeneracyjnych.
Badania dr Agnieszki Krzyżosiak i jej zespołu sugerują, że zaburzenia tych mechanizmów w astrocytach mogą stanowić kluczowy moment w rozwoju choroby. Naukowcy przypuszczają, że modulowanie procesów proteostazy w astrocytach może chronić neurony przed postępującą degeneracją.
Badaczka wykazała wcześniej skuteczność podobnego podejścia w pracach nad stwardnieniem zanikowym bocznym (ALS). Opracowana przez nią metoda farmakologicznego wzmacniania komórkowej odpowiedzi na stres doprowadziła do badań klinicznych u pacjentów z tą chorobą.
– Dzięki technologii pozwalającej przeprogramować komórki pobrane na przykład ze skóry pacjenta w komórki nerwowe możemy tworzyć modele mózgu zachowujące biologiczny wiek pacjenta. Możemy w laboratorium odtworzyć stan organizmu konkretnej, dorosłej osoby – wyjaśnia liderka Grupy Badawczej Mechanizmów Neurodegeneracji.
Tak precyzyjne podejście daje nadzieję na opracowanie terapii, które zamiast jedynie łagodzić objawy, mogłyby rzeczywiście zatrzymać degenerację całych sieci neuronowych poprzez przywrócenie prawidłowego funkcjonowania astrocytów.
Astrocyty w Centrum P4Health
Po dekadach skupiania się wyłącznie na neuronach patrzenie na mózg jako na złożony ekosystem otwiera zupełnie nowe możliwości w medycynie. Naukowcy dostrzegają w komórkach glejowych nową przestrzeń terapeutyczną – potencjał dla leków, które zamiast neuronów będą celować w astrocyty.
Zarówno zespół dr. Ślęzaka, jak i dr Krzyżosiak prowadzą swoje badania w ramach Centrum P4Health w Łukasiewicz – PORT. Wraz z oficjalnym uruchomieniem neuronaukowej Międzynarodowej Agendy Badawczej (MAB) pod koniec lutego, P4Health stało się jednym z niewielu ośrodków naukowych na świecie, które umieściły astrocyty w centrum swojego programu badawczo-rozwojowego.
Dzięki grantowi w wysokości 8 milionów euro z Fundacji na rzecz Nauki Polskiej wrocławski ośrodek zyskał kluczowe narzędzia do realizacji tej wizji. W kolejnych etapach projektu do instytutu mają dołączyć nowi naukowcy i nowe zespoły badawcze.
Na czele całego projektu MAB oraz jednej z nowych grup badawczych stoi prof. Bastian Hengerer. Jego zespół będzie rozwijał biomarkery translacyjne oraz wykorzystywał innowacyjną ultrasonografię funkcjonalną (fUS) do obserwowania i mierzenia, w jaki sposób leki lub modyfikacje genetyczne skierowane bezpośrednio na astrocyty mogą naprawiać zaburzone połączenia w sieciach neuronalnych mózgu.
Synergia wiedzy wszystkich liderów pozwoli badaczom w P4Health analizować astrocyty na wielu poziomach – od ekspresji genów w pojedynczych komórkach, przez złożone obwody neuronalne, aż po przedkliniczne testowanie nowych strategii terapeutycznych.
Trzeba jednak podkreślić: są to wciąż kierunki badań, a nie gotowe terapie. Samo wskazanie dysfunkcji gleju jako źródła chorób mózgu to dopiero początek. Kluczowym etapem przełożenia tych odkryć na praktykę kliniczną będą badania eksperymentalne, które pozwolą zweryfikować strategie terapeutyczne przywracające fizjologiczną funkcję astrocytów w modelach umożliwiających obiektywne pomiary biologiczne.




